研究概要RESEARCH
インフルエンザウイルスの増殖サイクル
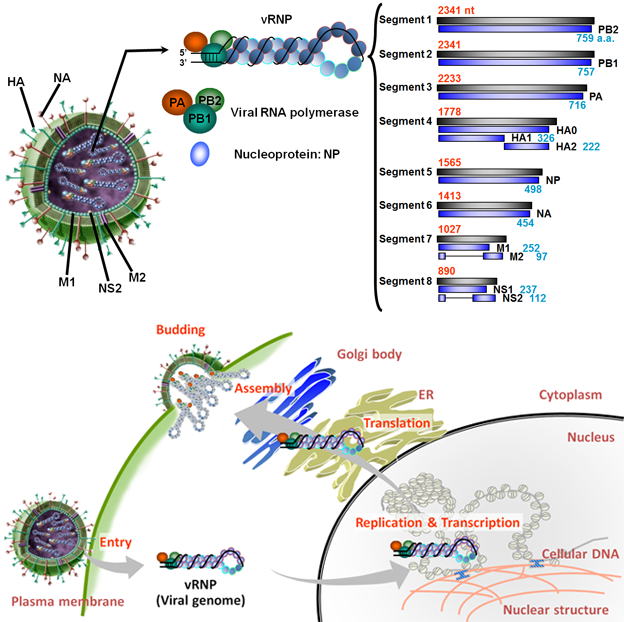
ヒトのゲノムは、22対の常染色体と1対の性染色体からなる、約31億塩基の2本鎖DNAです。
一方、インフルエンザウイルスは、8種類の一本鎖RNA(Segment 1〜8)をゲノムとして持つウイルスです。
最短で890塩基、最長のものでも2,341塩基しかなく、1本のウイルスゲノムには、1ないしは2個しかウイルス遺伝子はコードされていません。そのため、ウイルスは細胞への吸着・侵入(Entry)から出芽(Budding)まで、すべての増殖過程で、多くの細胞由来の因子(宿主因子)をハイジャックします。
ウイルスゲノムは、末端にウイルス由来のRNAポリメラーゼ(PB1、PB2、PA)複合体が、15〜25塩基ごとにNPが数珠状に結合し、viral
Ribonucleoprotein(vRNP)複合体とよばれる非常に大きな複合体を形成しています。
感染後、細胞質へ放出された各vRNP複合体は細胞核内へと移行し、ウイルスポリメラーゼによって、転写およびゲノム複製を行います(次項参照)。
インフルエンザウイルスのゲノム機能の制御機構
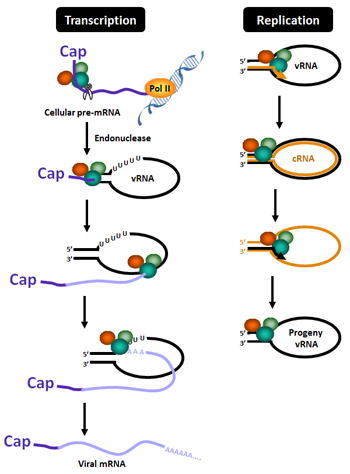
インフルエンザウイルスのゲノム(vRNA)は、マイナス鎖(遺伝子をコードするのがプラス鎖)の一本鎖RNAです。各Segment間で5’および3’末端側の十数塩基は部分的に相補的であり、ウイルスゲノムはパンハンドル(フライパンの柄)のような構造を取ります。この末端にウイルスポリメラーゼは結合し、ここから転写および複製は開始されます。
ウイルスポリメラーゼは、宿主pre-mRNAのキャップ構造を認識し、自身のエンドヌクレアーゼ活性により、キャップ構造から10〜13塩基下流を切断することができます。このキャップ構造をもつRNA断片をプライマーとして、転写反応は開始され、伸長後、vRNAの5’末端近傍のウラシル残基が連続した領域を反復して転写することで、約20〜30塩基のポリA鎖をウイルスmRNAに付加します。
一方、複製反応は、プライマー非依存的に開始され、vRNAから完全相補鎖のcomplementary RNA (cRNA)が合成され、このcRNAを鋳型に子孫vRNAが産生されます。
各反応には宿主因子が必須であり、我々は、試験管内でウイルスゲノムの転写・複製反応を再構成することで、各反応を促進する宿主因子の同定をすすめ(EMBO J., 2007; J Virol., 2011など)、宿主DNA複製のライセンシング因子であるMCMがウイルスゲノム複製の伸長反応に関与することやスプライシング因子のUAP56が子孫RNP複合体を形成するのに重要であることなどを明らかにしてきました。
また、ウイルスポリメラーゼの部分構造を明らかにすることにも成功し、さらに詳細な作用機構解析も展開しています(Nature, 2008; EMBO
J., 2009)。
ウイルスゲノムの転写と複製は、全くことなる機序で行われますが、用いられるウイルスポリメラーゼは同一のものであり、ウイルスポリメラーゼの機能調節機構が必須です。また、一部の高病原性株では、ウイルスポリメラーゼに変異が同定されており、それによって、種特異性(病原性?)が規定されている可能性が報告されています。
Ribonucleoprotein複合体の細胞内動態制御
感染細胞核内で複製されたウイルスゲノムは、vRNP複合体を形成し、宿主のExportinであるCRM1依存的に核外輸送されます。核外輸送されたvRNP複合体は、細胞膜の直下まで輸送され、ウイルス粒子に取り込まれて出芽します。
しかし、vRNP複合体の細胞内動態を制御する要因に関しては、これまで明らかにされていませんでした。
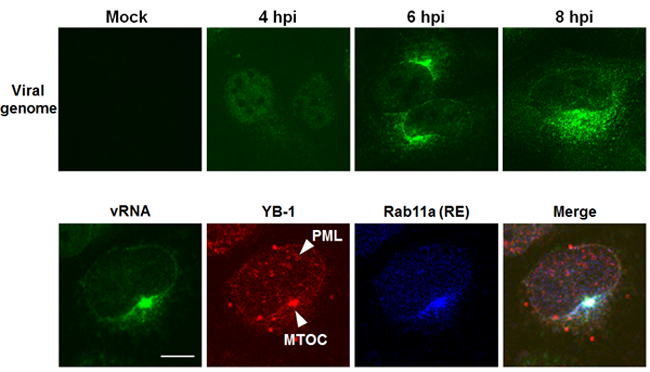
我々は、ウイルスゲノムを可視化することで、その細胞内動態を詳細に観察することで、vRNP複合体が輸送小胞(リサイクルエンドソーム)を介して、微小管依存的に細胞膜まで輸送されることを明らかにしました。
また、宿主mRNAの主要な構成因子であり、宿主mRNAの安定性や翻訳制御に関与する宿主因子であるYB-1は、PML(promyelocytic leukemia)bodyとよばれる核内ドメインに子孫vRNP複合体と集積し、vRNP複合体とともに核外輸送されること、ならびに、YB-1によって、核外輸送されたvRNP複合体はMicrotubule organizing center(MTOC)へ蓄積し、MTOCを介して微小管上の輸送小胞へリクルートされることを明らかにしています。
抗ウイルス薬の開発
インフルエンザウイルス感染症に対する抗ウイルス薬として、ウイルスの出芽を阻害するオセルタミビル(タミフル)や、ウイルスの脱殻を阻害するアマンタジンが上市されています。しかし、既にこれらの抗ウイルス薬に対して、抵抗性をもつウイルスが出現しており、これまでとは異なる阻害機構でウイルス増殖を抑制する抗ウイルス薬の開発が求められています。
我々は、横浜市立大学、産業技術総合研究所、東京都臨床医学総合研究所との共同研究で、独自の基礎研究から得られたデータをもとに、抗ウイルス薬の開発を展開しています。(特願2010-533938、特願2010-519109)
連絡先
〒305-8575
茨城県つくば市天王台1−1−1
筑波大学 医学医療系 感染生物学
(分子ウイルス学)
TEL 029-853-3942
FAX 029-853-3942

