リボソームプロファイリング(Ribo-Seq)
RNAは塩基の並び方によって区別でき、その配列によって異なった性質を持ちます。その数実に数万〜数十万種類ですが、これまでの研究ではそれらを1つ1つ個別に調べるしかありませんでした。しかし近年、次世代シーケンサーとよばれる機器が開発され、配列を一度に大量に決定できるようになりました(数億〜数十億回)。すると、配列からRNAの種類を、配列決定の回数からRNAの量を、網羅的に測定することができるようになってきました(トランスクリプトーム解析と呼ばれます)。
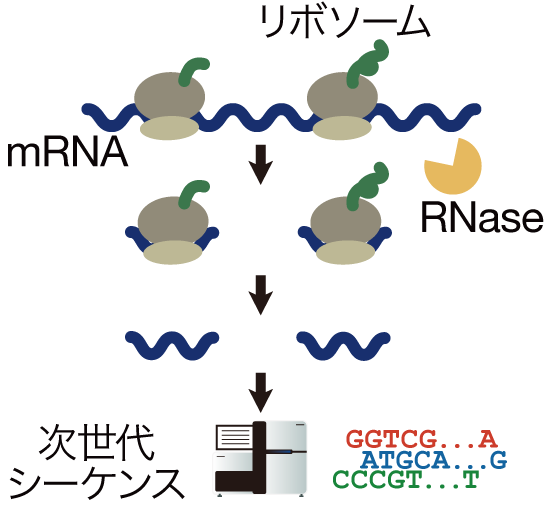
これを使ってmRNAの翻訳状況を網羅的に解析する手法がリボソームプロファイリング(Ribo-Seq)です。この手法では、まず細胞の抽出液を作り、RNA分解酵素(RNase)を加えます。すると、RNAはほぼ全て分解されてしまいますが、リボソームは固い構造を持っているので、リボソームが結合しているmRNAの領域は分解されずに残ります。そこで、残ったRNA断片を次世代シーケンサーで解析し、得られた配列データをコンピューターを使ってゲノム配列と照らし合わせれば、リボソームがどこにどれだけ結合していたか、つまりどのmRNAがどれだけ翻訳されていたかを網羅的に測定することができます。
私達の研究室では、この方法を主軸に、生化学や分子生物学手法、また蛍光顕微鏡観察などを組み合わせ、RNAの制御する生命現象の謎を解き明かしていきます。生化学・分子生物学実験(Wet)とコンピューター解析(Dry)の両方ができる二刀流の研究者を、研究室の全員が目指します。
局所翻訳の網羅的解析
翻訳は細胞内のどこで起こっているのでしょうか?真核生物では、核内で転写されたmRNAは細胞質に輸送され、そこでリボソームと出会い、翻訳が起こります。では、細胞質では均等に翻訳が起こっているのでしょうか?
最近の研究では、mRNAは細胞の特定の場所に運ばれ、そこで局所的な翻訳を受けることが知られています。局所翻訳は、少ないmRNA分子の輸送で多くのタンパク質分子を合成することができるため、タンパク質を作って運ぶのよりも効率よくタンパク質を局在化させる仕組みだと考えられています。例えば、ミトコンドリアでは、その膜の上で翻訳が起こり、タンパク質は作られているそばからミトコンドリアの中に送り込まれています。また、神経のような細長い細胞では、軸索などその先端部分での局所翻訳は細胞活動に重要で、局所翻訳の異常は神経疾患などと深いかかわりがあります。
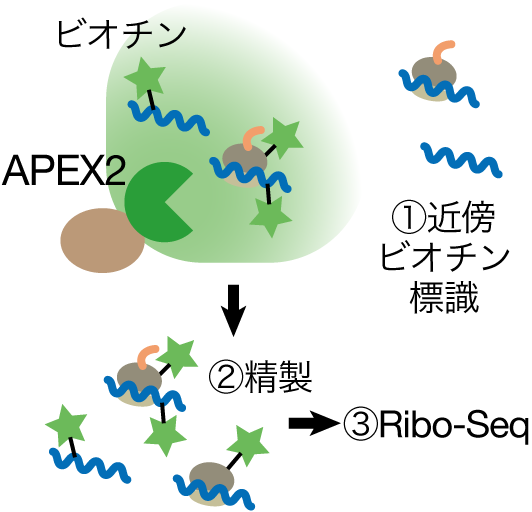
しかし、局所翻訳を網羅的に調べることは難しく、これまでどのmRNAが、どこで、どれくらい翻訳されているか、という情報は限られていました。私達の研究室では最近、APEX-Ribo-Seqという汎用的な局所翻訳の網羅的解析手法を開発し、14のオルガネラに適用した局所翻訳アトラスという大規模データセットを作成しました(プレプリント)。このデータを解析すると、これまでの研究ではわからなかった、局所翻訳の緻密な制御や、局所翻訳の生命における意義が見えつつあります。
では、局所翻訳はどのように制御されているのでしょうか?そして局所翻訳がおかしくなると生物はどうなってしまうのでしょうか?今後はこれら2つの疑問に重点を置き、網羅的な手法と顕微鏡観察を駆使して解答していきます。
非膜性オルガネラを介した翻訳制御
タンパク質は必要なときに必要なだけ作ることが大切です。いらないときにタンパク質を作ってしまうと、無駄になるばかりか、細胞に悪影響を及ぼすこともあります。ですので、mRNAは転写された後、翻訳すべきタイミングまでどこかで翻訳されないように保管されていなければいけません。
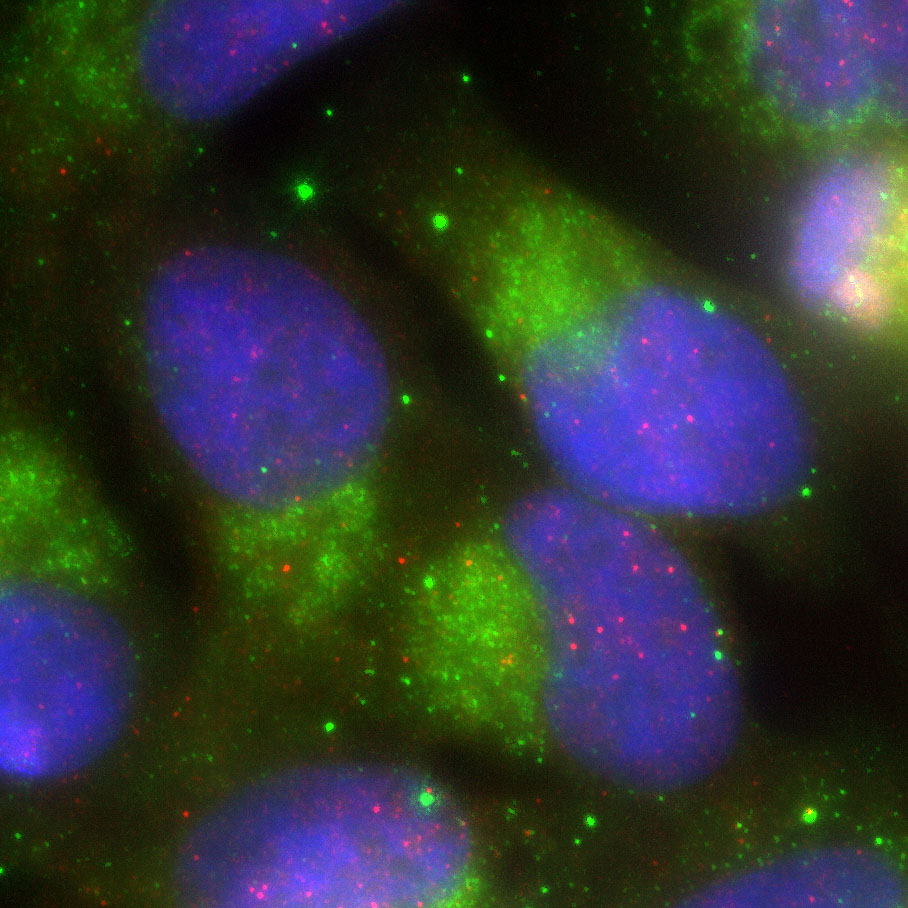
この保管機構に重要だと考えられているのが、RNAとタンパク質が凝集し合ってできる構造体であるRNP顆粒です。脂質膜を持たないため、非膜オルガネラとも呼ばれる構造体の一種です。細胞内には様々なRNP顆粒がありますが、その中身は実に様々で、疾患の細胞でしか観察できないものもあります。最近の研究では、このような構造体の中にmRNAを隔離し、翻訳を制御している可能性が示唆されています。
では、どうやってmRNAを出したり入れたりしているのでしょうか?そして、mRNAの局在制御は翻訳と関係しているのでしょうか?この仕組みが破綻すると細胞にどういう影響が出るのでしょうか?これらの疑問に対して、顆粒の生化学的精製・標識とRNA-Seqを組み合わせた顆粒トランスクリプトーム解析(総説)を行うことで解答していきます。
多彩な共同研究

Ribo-Seqを使った共同研究も多数展開しています。これまでに、ストレス応答、RNA修飾、免疫、神経・学習、発生・分化、老化、種内多様性などの生命現象における翻訳の制御機構と重要性を明らかにしてきました。また、生物種もヒトの不死化された培養細胞だけでなく、iPS細胞、出芽酵母、マウス個体やオルガノイド、ゼブラフィッシュ、ショウジョウバエ、植物、アメーバなど、多岐にわたります(抽出液を作ってしまえば同じように実験できます!)。今後も継続して多くの共同研究を展開し、研究ネットワークの構築を目指していきます。