悪性リンパ腫の非血液細胞を分類・カタログ化した単一細胞アトラスを作製
本研究結果は、悪性リンパ腫の治療開発やバイオマーカーの確立に寄与することが期待される他、今回作製された単一細胞アトラスは、広くがんおよびがん免疫研究の発展に資するプラットフォームになると考えられます。
〜複雑なゲノム編集変異を網羅的に解析する手法を開発〜<

実験用マウスの受精卵でのゲノム編集では、たった一塩基のみの意図した通りの改変や、目的の遺伝子領域の切除、少し離れた二箇所の染色体部位への他の生物種に由来する遺伝子配列の挿入が可能です。しかし、これらの「意図した遺伝子改変」を生じさせようとすると、標的としていない数塩基が欠失・挿入されてしまったり、想定を超える染色体領域が欠失・逆位となる「意図しない遺伝子改変」が起きたりすることもあります。困ったことに、意図した遺伝子改変が片側(母方もしくは父方)の染色体上で生じている時に、もう片側(父方もしくは母方)の染色体では意図しない遺伝子改変が起きることもあります。
意図した遺伝子改変マウス系統を実験に使用するためには、ゲノム編集を施された受精卵から発生した数十匹のマウスから「意図した改変遺伝子」を持つマウスを遺伝子検査で特定する必要があります。本研究で開発した遺伝子検査法では、約100匹のマウスのそれぞれでどのような遺伝子改変が生じたのか、網羅的かつ正確に、簡便に特定できます。この遺伝子検査手法はゲノム編集実験にかかる期間の短縮やその正確性の向上に寄与すると期待されます。
2022年 2月 11日
登録は締め切られました 。 イベントが完了しました 。
→
本シンポジウムへのご参加はZoomを用いて行います。
次 第
司会:TMRC 教授 杉山 文博
14:00〜14:05 学長挨拶
学長 永田 恭介 先生
14:05〜14:10 来賓祝辞
文部科学省 大学研究基盤整備課長
黒沼 一郎 様
14:10-14:30 筑波大学生命科学動物資源センター/TMRCの概要説明
TMRC長 高橋 智
記念シンポジウム
座長:高橋 智
14:30〜15:10
東京大学医科学研究所 および スタンフォード大学
教授 中内 啓光 先生
「iPS細胞から臓器をつくる:国境を跨いだ挑戦」
15:10〜15:50
慶応義塾大学 医学部
教授 岡野 栄之 先生
「iPS細胞と遺伝子改変霊長類技術を用いた医学研究」
15:50〜16:30
東北大学医学部および東北メディカルメガバンク機構
教授 山本雅之先生
「酸化ストレス応答の分子メカニズムと病態」
16:30〜17:10
筑波大学 国際睡眠医科学研究機構
教授 柳沢 正史 先生
「睡眠の謎に挑む 〜『眠気』の実体を求めて〜」
閉会の辞
TMRC 教授 杉山 文博
第18回(令和3(2021)年度)日本学術振興会賞 医学医療系 山﨑 聡
医学医療系の山﨑 聡 教授は、第18回(令和3年度)日本学術振興会賞を受賞しました。受賞の対象となった研究業績は「造血幹細胞の生体外における増幅法の確立」です。
 日本学術振興会賞は、創造性に富み優れた研究能力を有する若手研究者を見い出し、早い段階から顕彰することで、その研究意欲を高め、研究の発展を支援することにより、我が国の学術研究の水準を世界のトップレベルにおいて発展させることを目的としています。
日本学術振興会賞は、創造性に富み優れた研究能力を有する若手研究者を見い出し、早い段階から顕彰することで、その研究意欲を高め、研究の発展を支援することにより、我が国の学術研究の水準を世界のトップレベルにおいて発展させることを目的としています。
→ 日本学術振興会賞 の詳細については、ホームページをご覧ください。
→ 第18回(令和3年度)日本学術振興会賞受賞者及び授賞理由 (PDF JSPSのホームページ)
→ 山崎教授が率いるTMRCの幹細胞治療分野について。
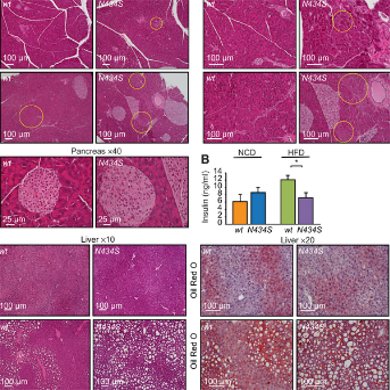
非アルコール性脂肪性肝炎をわずか3日で発症するマウス作成に成功
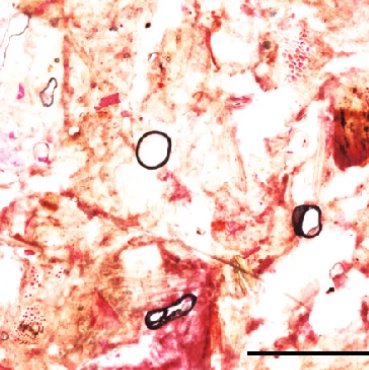
しかしながら、どのようにNASHが発症するのかは未だ分かっていません。そのため、動物モデルを利用し、偏った食生活や遺伝的背景などさまざまな要因を調べる研究が行われていますが、これまでのモデルの多くでは、NASHの発症を誘導するために一か月~一年という長期間が必要であるため、発症メカニズムを詳細に調べることが困難でした。
本研究グループは、先天的にメラニン色素が欠乏したアルビノ化を引き起こすチロシナーゼ遺伝子に着目し、この遺伝子に変異を持つアルビノマウスに高コレステロール食を与えると、わずか三日間で肝臓における脂質の蓄積、肝細胞の肥大、炎症細胞の浸潤、線維化等が起こり、ヒトのNASH病態がよく再現できることを発見しました。このマウスは、世界で最も短期間でNASHを発症するマウスモデルとして、NASH発症の遺伝的メカニズムの解明、新規の治療法の開発に活用されると期待されます。また今後、チロシナーゼ遺伝子とNASH発症の関連を調べることで、民族間でNASHの発症率が異なる原因などを説明できる可能性があります。
→ プレスリリース PDF
→
Scientific Reports 11, Article number: 21827 (2021)
DOI 10.1038/s41598-021-00501-5
Albino mice with the point mutation at the tyrosinase locus show high cholesterol diet-induced NASH susceptibility.
(チロシナーゼ遺伝子座に点変異を持つアルビノマウスは高コレステロール食誘導性 NASH
の感受性が高い)
メタボリックシンドロームを制御する代謝産物センサー分子を発見
本研究では、2つの代謝産物、糖を使ったエネルギー代謝と連動するNADHと、脂質を使ったエネルギー代謝と連動する脂肪酸CoAのバランスが重要で、それを認識するセンサー分子CtBP2が代謝を調節していることを明らかにしました。すなわち、健康な状態では、CtBP2はNADHと結合して活性化しており、肝臓では糖新生や脂質合成を抑え、糖尿病や脂肪肝にならないように働きますが、肥満になると、脂肪酸CoAが肝臓内で増加してCtBP2の機能を抑制し、糖新生や脂質合成が増加し、糖尿病や脂肪肝をもたらします。このメカニズムは、CtBP2の分子構造に基づくNADHや脂肪酸CoAの結合状態の解析からも裏付けられました。さらに、肥満の肝臓でCtBP2を活性化すると糖尿病や脂肪肝が劇的に改善することが分かりました。
本研究は、これまでにない形で代謝を理解するものであり、メタボリックシンドロームの新しい治療法開発の可能性を示唆しています。
→ プレスリリース PDF
→
Nature Communications 12, Article number: 6315 (2021)
DOI 10.1038/s41467-021-26638-5
The transcriptional corepressor CtBP2 serves as a metabolite sensor orchestrating
hepatic glucose and lipid homeostasis
(CtBP2は代謝産物センサーとして機能し、肝臓の糖・脂質代謝に重要な役割を果たしてい
る)
A common genetic variant of a mitochondrial RNA processing enzyme predisposes to insulin resistance
The findings revealed that the MRPP3 variant may be a predisposing factor to insulin resistance and metabolic disease in the human population.
→
doi/10.1126/sciadv.abi7514
酸化ストレスに対抗するタンパク質が微小重力下での筋線維タイプの変化を抑制する

そこで本研究では、Nrf2が宇宙環境における酸化ストレスの防御にも有効ではないかと考え、国際宇宙ステーション(ISS)の「きぼう」実験棟の微小重力環境において、野生型およびNrf2遺伝子ノックアウトマウスを31日間飼育し、骨格筋に与える影響を調べました。重力変化に対して感受性の高いヒラメ筋に着目し、遺伝子発現解析および組織学的解析した結果、微小重力環境によるヒラメ筋の萎縮には違いは見られませんでしたが、筋線維タイプの変化については、Nrf2遺伝子ノックアウトマウスで大きくなっていました。このことから、Nrf2が、微小重力環境下で生じる筋線維タイプの変化を抑制することが分かりました。
筋線維タイプの変化は、宇宙滞在や老化に伴って生じるものであり、本研究成果をもとに、その分子メカニズムを解明できれば、こういった症状の予防や治療方法の確立につながると期待されます。
→ プレスリリース PDF
→
Communications Biology volume 4, Article number: 787 (2021)
DOI 10.1038/s42003-021-02334-4
Nuclear factor E2-related factor 2 (NRF2) deficiency accelerates fast fibre type transition in soleus muscle during space flight.
(NRF2 の欠損は、宇宙飛行中のヒラメ筋の速筋線維
タイプの移行を加速する。)
マウスの心筋は心筋直接リプログラミングで心臓線維芽細胞から真に再生することを証明
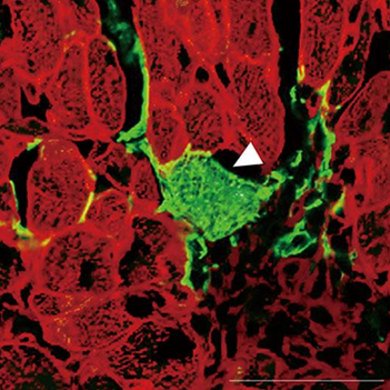
本研究グループは、これまでに、これらの課題を解決し得る別の方法として、幹細胞を用いずに心臓線維芽細胞から直接心筋細胞を誘導する「心筋直接リプログラミング法」を開発しています。しかしながら、生体内の心臓線維芽細胞に心筋リプログラミング遺伝子を導入して作製する心筋細胞が、真に心臓線維芽細胞由来の誘導された再生心筋細胞か、あるいは心臓線維芽細胞と周囲の心筋細胞が融合してできた見かけ上再生して見える心筋細胞かは不明でした。そこで本研究では、細胞の系譜と融合を明らかにする遺伝子改変マウスを用いて、生体内で新たに作製された心筋細胞が、心臓線維芽細胞由来の真の再生心筋細胞であることを、世界で初めて明らかにしました。
本研究により、マウス生体内に心筋リプログラミング遺伝子を導入することで、心臓線維芽細胞から直接心筋細胞を誘導できることが分かりました。本研究結果は心疾患に対する新しい心臓再生医療の実現を大きく前進させることが期待されます。
→ プレスリリース PDF
→
(Gata4, Mef2c, Tbx5過剰発現は心筋直接リプログラミングと低頻度の細胞融合により心筋
再生する)
Circulation 143:2123–2125(2021)